ASOURCE®NAVI

公開日:2022.03.17
海外製の新型コロナウイルスワクチン接種が進むなか、利便性や安全性を生かした独自の開発を進めてきた日本の製薬メーカーによるワクチンが、いよいよ実用化される見通しです。
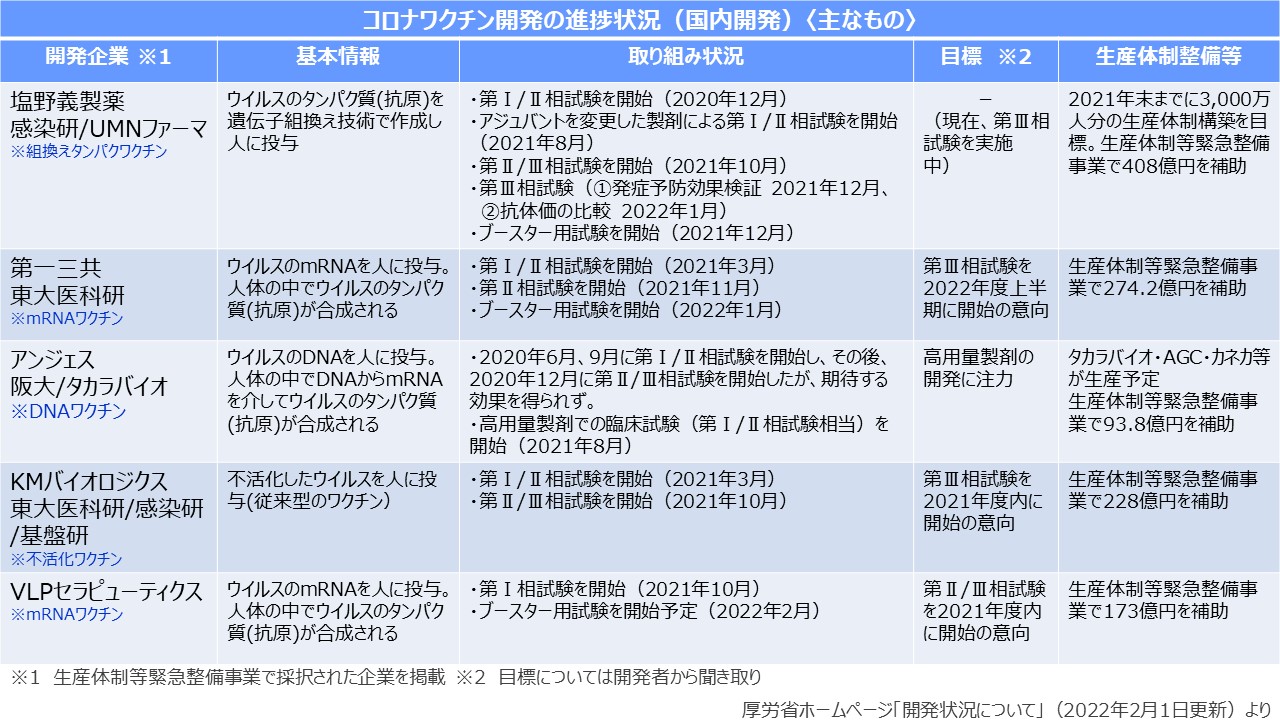
国内のコロナワクチン開発で先行している塩野義製薬は、未接種者向けの臨床試験よりも追加接種での使用を想定した臨床試験を優先させています。このワクチンは、ウイルスの遺伝子情報からワクチンのもととなる物質(抗原タンパク質)を作る組み換えタンパクワクチンで、すでに帯状疱疹などのワクチンに使われています。このほど公表された追加接種の第2/3相臨床試験の中間報告では、ファイザー製と比較して有効性は同等で、発熱や頭痛などの副反応は低いことが示されました。
この臨床試験では、ファイザー製のワクチンを2回接種して6カ月以上経過した国内の成人約200人を対象に、追加接種として開発中のワクチンを接種した群とファイザー製のワクチンを接種した群とで有効性と安全性を比較しました。その結果、開発中のワクチン接種群は、ファイザー製ワクチン接種群との比較で接種約1カ月後の中和抗体価が1.17倍となっており、有効性は同等であることが確認されました。また、副反応の発現率は、開発中のワクチンがファイザー製よりも発熱(塩野義製:38.8%、ファイザー製:59.2%)、頭痛(塩野義製:25.2%、ファイザー製:41.7%)、倦怠感(塩野義製:43.7%、ファイザー製:53.4%)などで低いことが示されました。接種部位の痛みや筋肉痛も塩野義製がファイザー製と比べて同等以下でした。この結果を踏まえて、同社では承認申請の準備を進め、今年5月以降の供給開始を目指す方針としています。一方、未接種者向けの最終段階の臨床試験は、国内では人口の8割がワクチン接種済み(2回接種完了)のため、未接種者の多いベトナムなど東南アジアの国で約5万人を対象に実施中とされます。
既に一般への接種が始まっているファイザー製などと同じメッセンジャーRNA(mRNA)を用いたワクチンを開発中の第一三共は、従来の開発方針を改め、今年から追加接種の臨床試験を先行してスタートさせ、年内の供給を急いでいます。これに伴い、未接種者向けの最終段階の臨床試験は延期することにしました。ファイザー製ワクチンは超低温冷凍の保存が必要ですが、第一三共製は冷蔵保存できるワクチンを目指しています。KMバイオロジクスも追加接種の臨床試験を医師主導の形で進めています。開発しているのはインフルエンザワクチンと同じウイルスの感染力を無くした不活化ワクチンで、同社はこれまでの長期の使用実績から安全性が担保されている、としています。
アンジェスは、ウイルスの遺伝子情報を導入したプラスミドDNAを投与するワクチンをいち早く開発していましたが、当初設計した用量の製剤を見直し、高用量製剤での開発に切り替えたため開発が大幅に遅れ、供給開始は2023年頃と見込まれています。VLPセラピューティクスは、少量の接種で効果が期待できる新しいタイプのコロナワクチンを開発中で、昨年10月に初期段階の臨床試験を開始しています。このワクチンは、接種後に体内で増える自己増殖型と呼ばれるメッセンジャーRNA(mRNA)で、ファイザー製やモデルナ製と比べて接種量が10分の1〜100分の1で済むのが特徴で、副反応が軽減される可能性があるとされます。一方、田辺三菱製薬は、カナダの子会社(メディカゴ)が開発した植物由来のワクチンについて、国内の未接種者に対して臨床試験を進めており、今秋までに承認申請を目指しています。このワクチンは、植物の葉にウイルスの遺伝子を組み込み、ワクチンの成分を抽出したもので、2回接種後の発熱の頻度は10%未満で、追加接種の臨床試験も検討しています。
医薬品の研究開発において有効性を重視する欧米と安全性を重視する日本という違いがあるとされますが、コロナワクチンの開発においてもその“文化の違い”が色濃く反映されているようです。
メディアスグループは、医療機器の販売を中心とした事業を展開しています。医療に携わる私たち(Medical+us)は、医療現場や人々の健康的な明日へ役立つ情報をお届けする情報発信源(Media)の役割も果たしていきたいと考えています。